Cientistas da Fundação Oswaldo Cruz (Fiocruz) lideram um esforço nacional de pesquisa que busca decodificar o genoma do SARS-CoV-2, causador da Covid-19, e acompanhar suas linhagens e mutações genéticas. Por meio da Rede Genômica Fiocruz, especialistas de todas as unidades da Fundação no país e de institutos parceiros se empenham diariamente em gerar dados mais robustos sobre o comportamento do vírus e contribuir para um melhor preparo do país no enfrentamento da pandemia em termos de diagnóstico mais precisos e vacinas eficazes.
O grupo participa da iniciativa internacional de acesso aberto a informações sobre genomas de vírus influenza e coronavírus, o GISAID. Desde o início da pandemia, mais de 524 mil sequências genômicas do novo coronavírus já foram compartilhadas por pesquisadores de todo o mundo.
Com foco na situação do Brasil, a Rede Genômica Fiocruz passou a disponibilizar dados exclusivos do país no website da iniciativa. “Para o rápido progresso no entendimento da Covid-19 e suas complicações é fundamental estreitar a colaboração científica. Por meio dos dados genômicos é possível avançar em pesquisa e desenvolvimento de possíveis vacinas e medicamentos, além de manter os kits de diagnóstico sempre atualizados com os genomas circulantes e a vigilância da dispersão dos vírus sempre alerta, ainda mais em um momento em que está sendo observado o surgimento de variantes do novo coronavírus", frisa a chefe do Laboratório de Vírus Respiratórios e do Sarampo do Instituto Oswaldo Cruz (IOC/Fiocruz), Marilda Siqueira, que atua como Centro de Referência Nacional em vírus respiratórios junto ao Ministério da Saúde e como referência para a Organização Mundial da Saúde em Covid-19 nas Américas.
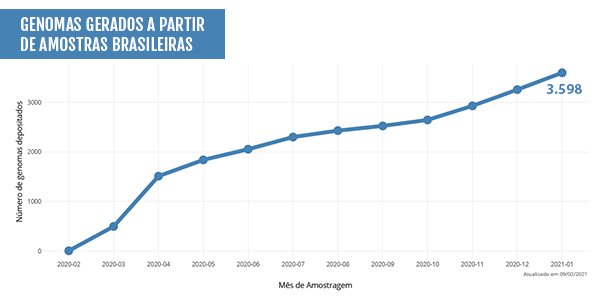
De acordo com os dados disponíveis no site da Rede Genômica Fiocruz, já foram realizados cerca de 3,6 mil sequenciamentos do genoma do SARS-CoV-2 no Brasil, sendo São Paulo o estado com o maior número de amostras sequenciadas, com um total de 1.035, seguido por Rio de Janeiro, com 726, Amazonas, 340, Rio Grande do Sul, 306, Paraíba, 167, e Pernambuco, com 150.
“Quanto maior for o investimento na ciência, mais rápidas serão as respostas ao atual e a futuros problemas de saúde pública”, salienta a coordenadora da curadoria da plataforma genômica GISAID no Brasil, a pesquisadora Paola Cristina Resende, do mesmo Laboratório.
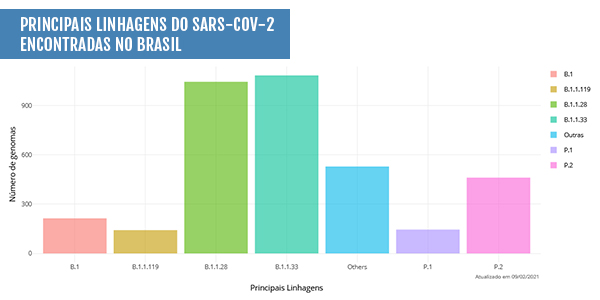
Segundo a iniciativa, mais de 60 linhagens do novo coronavírus já foram identificadas no país. No entanto, os especialistas destacam o predomínio das linhagens B.1.1.33 e B.1.1.28, que apresentam circulação nacional desde março de 2020. A linhagem B.1.1.28 deu origem a duas linhagens que passaram a circular mais recentemente no país, a P.1 e a P.2, denominadas cientificamente de “variantes de preocupação”, ou variant of concern (VOC), na expressão em inglês.
“A identificação da circulação de linhagens não tem ligação direta com gravidade da doença, aumento da transmissibilidade do patógeno ou impacto na eficácia das vacinas. No caso dos vírus, por exemplo, a maioria das mutações não causa mudanças na capacidade de dispersão ou infecção. O SARS-CoV-2 muda mais rapidamente que outros microrganismos, como bactérias e fungos. Na maior parte dos casos, as linhagens são distintas por pequenas diferenças em seu material genético, que podem não ser associadas a novas características virais”, explica Marilda.
No estado mais populoso do país, São Paulo, as variantes B.1.1.28 e B.1.1.33 são, até o momento, as que apresentam maior número de identificação. Já no Rio de Janeiro, a B.1.1.33 apresentou maior prevalência por um período. No entanto, nos últimos meses, a cepa P.2 tem demonstrado crescimento no estado, assim como em todo o país.
Em relação ao Amazonas, que enfrenta sérios problemas em seu sistema de saúde, os dados indicam o avanço acelerado da linhagem P.1. A recente variante, derivada de uma das linhagens que predominava no país, a B.1.1.28, é responsável atualmente por mais de 91% das infecções no estado. Estudos indicam que a variante contém pelo menos três mutações (K417N, E484K e N501Y), que afetam a proteína Spike, associada à entrada do vírus nas células humanas. A P.1 também foi identificada no Pará, Roraima, Paraíba, São Paulo e Santa Catarina. Confira o artigo sobre a relação filogenética de sequências de SARS-CoV-2 do Amazonas com as variantes emergentes brasileiras que abrigam mutações.
“Com o objetivo de detectar a circulação desta linhagem entre a população do Amazonas e outros estados do país, estamos recebendo de 30 a 40 amostras positivas de diferentes localidades para realizarmos o sequenciamento e entendermos a possível dispersão dessa e de outras cepas”, explica Fernando Motta, pesquisador do mesmo Laboratório. “Estão sendo conduzidos estudos com amostras isoladas das diferentes linhagens a fim de identificar como as mutações recém descritas podem afetar ou não a reposta induzida pelas vacinas em uso”, completa o virologista.
“É importante lembrar que as linhagens P.1 e P.2 já foram associadas a casos de reinfecção no país. Por isso, é fundamental a continuidade das medidas de prevenção, como a utilização de máscara de proteção, a higienização frequente das mãos e evitar aglomerações”, ressalta Paola. Confira detalhes aqui e aqui.
“Assim como há décadas existe uma rede de vigilância nacional muito bem estruturada para acompanhamento dos vírus influenza, causadores da gripe, que circulam em todo o mundo e sofrem mutações frequentes, nossa rede permanecerá igualmente empenhada nas vigilâncias epidemiológica e laboratorial do novo coronavírus, fundamentais para a formulação de vacinas sempre atualizadas e eficazes, por exemplo”, ressalta Marilda.
A Rede Genômica Fiocruz integra pesquisadores de todas as unidades da Fundação no país: Instituto Aggeu Magalhães (Fiocruz-PE), Instituto Gonçalo Moniz (Fiocruz-BA), Instituto René Rachou (Fiocruz-MG), Instituto Carlos Chagas (Fiocruz-PR), Instituto Leonidas e Maria Deane (Fiocruz-AM), assim como as unidades no Mato Grosso do Sul, Rondônia, Piauí e Ceará. Também participam especialistas do Instituto Oswaldo Cruz (IOC/Fiocruz), Instituto Nacional de Controle de Qualidade em Saúde (INCQS/Fiocruz), Instituto Nacional de Saúde da Mulher, da Criança e do Adolescente Fernandes Figueira (IFF/Fiocruz), além do Instituto Adolfo Lutz, de São Paulo, e Instituto Evandro Chagas, do Pará.
Cientistas da Fundação Oswaldo Cruz (Fiocruz) lideram um esforço nacional de pesquisa que busca decodificar o genoma do SARS-CoV-2, causador da Covid-19, e acompanhar suas linhagens e mutações genéticas. Por meio da Rede Genômica Fiocruz, especialistas de todas as unidades da Fundação no país e de institutos parceiros se empenham diariamente em gerar dados mais robustos sobre o comportamento do vírus e contribuir para um melhor preparo do país no enfrentamento da pandemia em termos de diagnóstico mais precisos e vacinas eficazes.
O grupo participa da iniciativa internacional de acesso aberto a informações sobre genomas de vírus influenza e coronavírus, o GISAID. Desde o início da pandemia, mais de 524 mil sequências genômicas do novo coronavírus já foram compartilhadas por pesquisadores de todo o mundo.
Pesquisadores já conseguiram sequenciar quase 3,6 mil amostras brasileiras
Com foco na situação do Brasil, a Rede Genômica Fiocruz passou a disponibilizar dados exclusivos do país no website da iniciativa. “Para o rápido progresso no entendimento da Covid-19 e suas complicações é fundamental estreitar a colaboração científica. Por meio dos dados genômicos é possível avançar em pesquisa e desenvolvimento de possíveis vacinas e medicamentos, além de manter os kits de diagnóstico sempre atualizados com os genomas circulantes e a vigilância da dispersão dos vírus sempre alerta, ainda mais em um momento em que está sendo observado o surgimento de variantes do novo coronavírus", frisa a chefe do Laboratório de Vírus Respiratórios e do Sarampo do Instituto Oswaldo Cruz (IOC/Fiocruz), Marilda Siqueira, que atua como Centro de Referência Nacional em vírus respiratórios junto ao Ministério da Saúde e como referência para a Organização Mundial da Saúde em Covid-19 nas Américas.
De acordo com os dados disponíveis no site da Rede Genômica Fiocruz, já foram realizados cerca de 3,6 mil sequenciamentos do genoma do SARS-CoV-2 no Brasil, sendo São Paulo o estado com o maior número de amostras sequenciadas, com um total de 1.035, seguido por Rio de Janeiro, com 726, Amazonas, 340, Rio Grande do Sul, 306, Paraíba, 167, e Pernambuco, com 150.
“Quanto maior for o investimento na ciência, mais rápidas serão as respostas ao atual e a futuros problemas de saúde pública”, salienta a coordenadora da curadoria da plataforma genômica GISAID no Brasil, a pesquisadora Paola Cristina Resende, do mesmo Laboratório.
Segundo a iniciativa, mais de 60 linhagens do novo coronavírus já foram identificadas no país. No entanto, os especialistas destacam o predomínio das linhagens B.1.1.33 e B.1.1.28, que apresentam circulação nacional desde março de 2020. A linhagem B.1.1.28 deu origem a duas linhagens que passaram a circular mais recentemente no país, a P.1 e a P.2, denominadas cientificamente de “variantes de preocupação”, ou variant of concern (VOC), na expressão em inglês.
O sequenciamento permite identificar todas as características genéticas do vírus, conhecimento fundamental para a formulação de vacinas e fármacos
“A identificação da circulação de linhagens não tem ligação direta com gravidade da doença, aumento da transmissibilidade do patógeno ou impacto na eficácia das vacinas. No caso dos vírus, por exemplo, a maioria das mutações não causa mudanças na capacidade de dispersão ou infecção. O SARS-CoV-2 muda mais rapidamente que outros microrganismos, como bactérias e fungos. Na maior parte dos casos, as linhagens são distintas por pequenas diferenças em seu material genético, que podem não ser associadas a novas características virais”, explica Marilda.
No estado mais populoso do país, São Paulo, as variantes B.1.1.28 e B.1.1.33 são, até o momento, as que apresentam maior número de identificação. Já no Rio de Janeiro, a B.1.1.33 apresentou maior prevalência por um período. No entanto, nos últimos meses, a cepa P.2 tem demonstrado crescimento no estado, assim como em todo o país.
Em relação ao Amazonas, que enfrenta sérios problemas em seu sistema de saúde, os dados indicam o avanço acelerado da linhagem P.1. A recente variante, derivada de uma das linhagens que predominava no país, a B.1.1.28, é responsável atualmente por mais de 91% das infecções no estado. Estudos indicam que a variante contém pelo menos três mutações (K417N, E484K e N501Y), que afetam a proteína Spike, associada à entrada do vírus nas células humanas. A P.1 também foi identificada no Pará, Roraima, Paraíba, São Paulo e Santa Catarina. Confira o artigo sobre a relação filogenética de sequências de SARS-CoV-2 do Amazonas com as variantes emergentes brasileiras que abrigam mutações.
“Com o objetivo de detectar a circulação desta linhagem entre a população do Amazonas e outros estados do país, estamos recebendo de 30 a 40 amostras positivas de diferentes localidades para realizarmos o sequenciamento e entendermos a possível dispersão dessa e de outras cepas”, explica Fernando Motta, pesquisador do mesmo Laboratório. “Estão sendo conduzidos estudos com amostras isoladas das diferentes linhagens a fim de identificar como as mutações recém descritas podem afetar ou não a reposta induzida pelas vacinas em uso”, completa o virologista.
“É importante lembrar que as linhagens P.1 e P.2 já foram associadas a casos de reinfecção no país. Por isso, é fundamental a continuidade das medidas de prevenção, como a utilização de máscara de proteção, a higienização frequente das mãos e evitar aglomerações”, ressalta Paola. Confira detalhes aqui e aqui.
“Assim como há décadas existe uma rede de vigilância nacional muito bem estruturada para acompanhamento dos vírus influenza, causadores da gripe, que circulam em todo o mundo e sofrem mutações frequentes, nossa rede permanecerá igualmente empenhada nas vigilâncias epidemiológica e laboratorial do novo coronavírus, fundamentais para a formulação de vacinas sempre atualizadas e eficazes, por exemplo”, ressalta Marilda.
A Rede Genômica Fiocruz integra pesquisadores de todas as unidades da Fundação no país: Instituto Aggeu Magalhães (Fiocruz-PE), Instituto Gonçalo Moniz (Fiocruz-BA), Instituto René Rachou (Fiocruz-MG), Instituto Carlos Chagas (Fiocruz-PR), Instituto Leonidas e Maria Deane (Fiocruz-AM), assim como as unidades no Mato Grosso do Sul, Rondônia, Piauí e Ceará. Também participam especialistas do Instituto Oswaldo Cruz (IOC/Fiocruz), Instituto Nacional de Controle de Qualidade em Saúde (INCQS/Fiocruz), Instituto Nacional de Saúde da Mulher, da Criança e do Adolescente Fernandes Figueira (IFF/Fiocruz), além do Instituto Adolfo Lutz, de São Paulo, e Instituto Evandro Chagas, do Pará.
Permitida a reprodução sem fins lucrativos do texto desde que citada a fonte (Comunicação / Instituto Oswaldo Cruz)
